こんにちは。サプリメントの製造・販売をしている株式会社ナックスです。今回は、抗酸化物質の機能性を向上させる還元型E-TENとビタミンCの組合せの最適化試験について書いていきます。
まず、還元型E-TENとは、「人は、呼吸で酸素を取り込み、食べ物を食べて栄養素(特に電子)を体内に取り入れ、酸化還元反応(電子のやり取り)することによってエネルギーを獲得しています。」そこでエネルギーを効率よく獲得するために電子が必要と考え安心・安全な素材で電子を供給する「還元型E-TEN」を開発しました。
還元型E-TENの製品案内は、下記の通りURLに記載しています。
ビタミンCの抗酸化作用の反応機構に関して
このブログを見て頂いている方は、何度かご説明させて頂いていますが、もう一度ご説明させていただきます。ビタミンCの抗酸化作用の反応機構についてご説明させていただきます。
下記の図は、ビタミンCの構造となります。
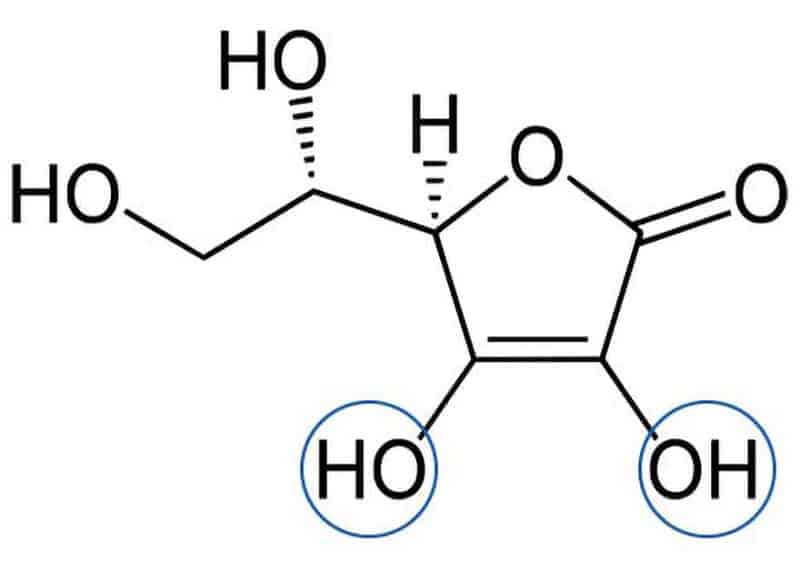
L-アスコルビン酸(ビタミンC)の抗酸化力は下記の図にて青丸で囲んだのがビタミンCの電子を供給する(抗酸化作用)ところを示すところです。ビタミンCは、1分子に2個の電子(2e-)を有しています。分子量から求めると1g当たりのビタミンCの還元力(抗酸化力)は、0.68×1022個となります。
NAD+試験によるビタミンCの電子の放出について
この試験は、中性下でNAD+が反応することによりNADHになった時、抗酸化物質が抗酸化作用及び電子が放出したかを見る反応となります。
実験条件は、下記の通りになります。
実験概要及び実験条件
還元型E-TENの還元力を測定方法は、NAD+試験方法を用いて行いました。NADH水溶液は、340nm付近にてピークが出現し、NAD+水溶液は、340nm付近で存在しません。これによりNAD+水溶液と還元型E-TENを反応させた溶液は、下記の図でわかるように340nm付近でピークが存在しています。このことからNAD+水溶液がNADH水溶液に変化していることがわかります。このことから下記の反応式が成り立ちます。
NAD+ + (2e– + H+) → NADH
準備
- NAD+1mmol/L水溶液・・・・NAD+0.0663gを精製水100mlにて調整
- NADH0.5mmol/L水溶液・・・NADH0.0035gを精製水10mlにて調整
- NAD+1mmol/L水溶液15mlに還元型E-TEN0.03g投入した溶液
山梨県産業技術センターの紫外可視分光光度計(株式会社島津製作所)にて測定。結果は下記の通りになります。
下の図は、NAD+1mmol/L溶液の結果となります。
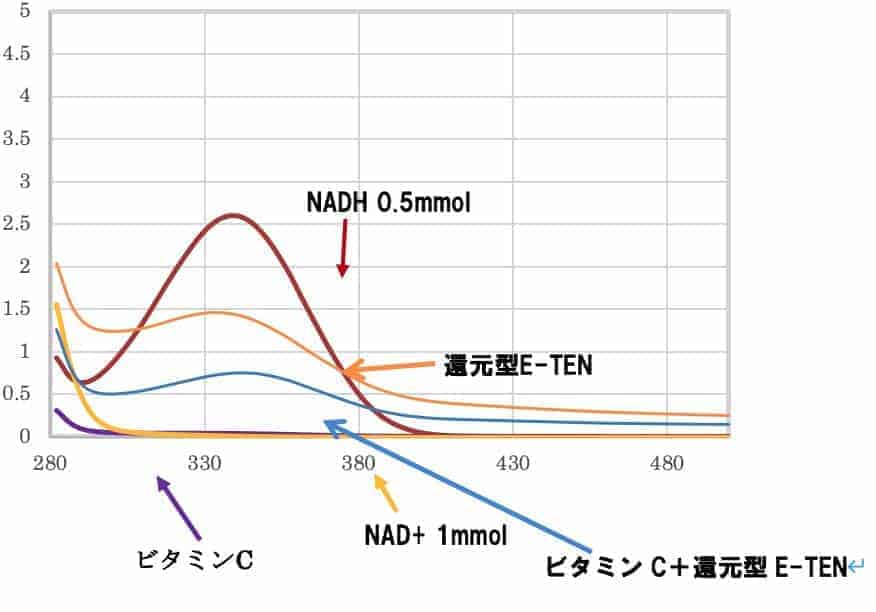
NADHは、波長340nmの紫外線をよく吸収しますがNAD+は、波長340nmで吸収しないため、ピークが存在しない。次にNADH0.5mmol/L水溶液は、波長340nmの紫外線をよく吸収するためピークが存在しています。
- NAD+1mmol/L水溶液15mlに還元型E-TEN0.03g投入した溶液
- NAD+1mmol/L水溶液15mlにビタミンC水溶液を投入した溶液
- NAD+1mmol/L水溶液15mlにビタミンC水溶液+還元型E-TENを投入した溶液
ビタミンCが単体で反応すれば効率良く体内でも抗酸化作用及び電子の放出が簡単に行われ体内での効果も期待できると考えられます。上記の図に関して、解説していきます。
赤い線は、NADH水溶液の結果となります。この赤い線に近づいた時に反応がNADHの水溶液になります。ビタミンCは、ピークはでず、NAD+溶液と同じ線となっていますので反応していないことがわかります。
ビタミンCと還元型E-TENを混ぜた水溶液では、NADHの水溶液になっていることがわかります。この結果から還元型E-TENがビタミンCの抗酸化作用及び電子の放出を促しているのがわかります。そのことにより還元型E-TENは、抗酸化物質の抗酸化作用及び電子の放出を促すことができると考えられます。
次にこの実験だけでは、本当に抗酸化物質の抗酸化作用及び電子の放出がわかりませんので、違う実験を行い、抗酸化作用及び電子の放出について書いていきます。
酸化還元電位とは
最初に酸化還元電位とは、電子のやり取りの際に発生する電位のことで、物質の電子の放出しやすさ、あるいは受け取りやすさを定量的に評価する尺度でもあります。
今回の測定にて簡単に書きますと水溶液中に溶け込んでいる酸化体と還元体の濃度比により決まるものとなります。イメージしにくいと思いますので下記の図にて説明させていただきます。
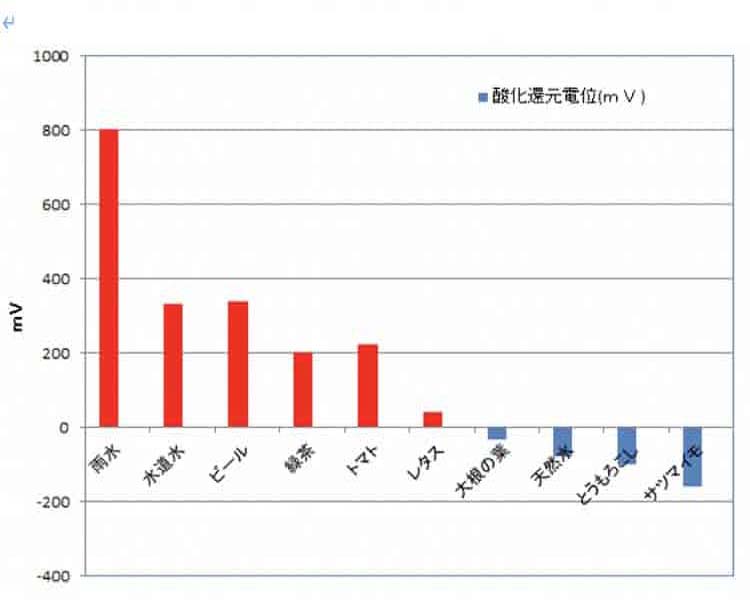
雨水、水道水、ビールは、高い酸化還元電位が高くなります。これは酸化体の物質が多く含んでいるので電子の消費が激しくなります。電子の消費が激しいと必要な電子が人体に使われず、エネルギーにならなくなります。この図により高い数値だと悪いということがわかります。
酸化還元電位を用いた還元型E-TENとビタミンCの最適化検討試験
実際に酸化還元電位の測定を行った結果を下記に書いていきます。
実験条件
下記の配合にて1時間後、7時間後、24時間後の酸化還元電位の測定を行いました。
- ビタミンC 100% 1gに精製水100ml
- ビタミンC 75% + 還元型E-TEN 25% 0.75g + 0.25gに精製水100ml
- ビタミンC 50% + 還元型E-TEN 50% 0.5g + 0.5gに精製水100ml
- ビタミンC 40% + 還元型E-TEN 60% 0.4g + 0.6gに精製水100ml
- ビタミンC 30% + 還元型E-TEN 70% 0.3g + 0.7gに精製水100ml
- ビタミンC 25% + 還元型E-TEN 75% 0.25g + 0.75gに精製水100ml
- ビタミンC 20% + 還元型E-TEN 80% 0.2g + 0.8gに精製水100ml
- ビタミンC 10% + 還元型E-TEN 90% 0.1g + 0.9gに精製水100ml
- 還元型E-TEN 1gに精製水100ml
測定結果
下記の表はそれぞれの酸化還元電位の測定結果となります。
| 0時間後 | 1時間後 | 7時間後 | 24時間後 | |
|---|---|---|---|---|
| ビタミンC 100% | 216 | 109 | 45 | 103 |
| ビタミンC 75%+還元型E-TEN 25% | 216 | -111 | -123 | -115 |
| ビタミンC 75%+還元型E-TEN 25% | 216 | -139 | -209 | -113 |
| ビタミンC 40%+還元型E-TEN 60% | 216 | -229 | -320 | -252 |
| ビタミンC 30%+還元型E-TEN 70% | 216 | -304 | -362 | -333 |
| ビタミンC 25%+還元型E-TEN 75% | 216 | -340 | -416 | -355 |
| ビタミンC 20%+還元型E-TEN 80% | 216 | -343 | -366 | -334 |
| ビタミンC 10%+還元型E-TEN 90% | 216 | -305 | -360 | -312 |
| 還元型E-TEN 100% | 216 | -126 | -148 | -183 |
還元型E-TENは、還元方向(マイナス側)なので抗酸化作用及び電子が放出していると考えられます。また、還元型E-TENとビタミンCを組み合わせることによって抗酸化作用及び電子が放出していることがわかります。
ビタミンCの効果が発揮するのは、ビタミンC25%+還元型E-TEN75%の組合せの時になります。こと時により多くの電子が放出することが考えられます。
還元型E-TENに関してのまとめ
還元型E-TENの電子の放出機構と還元型E-TENと他の抗酸化物質を組み合わせることによって電子の放出を促す効果があることがわかりました。還元型E-TENは、単体でも期待できる効果はありますが他の抗酸化物質と組み合わせることにより効果が期待できるのがわかります。
また、表よりビタミンCとの組合せの最適もわかります。より良いベストの製品の製造に参考にしていただければと思います。
化学的な実験を行いながら身体との関係について今後かいていきます。
還元型E-TENにご興味のある方は、お気軽にお問い合わせください。














